- DONALD
- NAUKOWCY Z UJ OPRACOWALI SPECJALNY ŻEL, KTÓRY MOŻE BYĆ PRZEŁOMEM W LECZENIU OSTEOPOROZY
Naukowcy z UJ opracowali specjalny żel, który może być przełomem w leczeniu osteoporozy
11.02.2023, 13:30

Naukowcy z
Wydziału Chemii Uniwersytetu Jagiellońskiego
opracowali materiał, który pomoże
odbudowywać ubytki kostne
i jednocześnie może służyć jako
nośnik leków na osteoporozę
. Przeznaczeniem wytworzonego materiału jest udoskonalenie metod leczenia osteoporozy oraz niwelowanie niedużych ubytków kostnych. Ma on postać hydrożelu wstrzykiwanego w miejsce ubytku kości. Tam dochodzi do jego "zestalenia" w wyniku sieciowania chemicznego zachodzącego w temperaturze 37ºC. Przyczepia się on do tkanki kostnej i pełni funkcję rusztowania, na którym w naturalnych procesach biologicznych tworzy się nowa tkanka kostna.
Oprócz tego
hydrożel
ma dodatkową właściwość. Może on być nośnikiem leków na osteoporozę, które da się podać miejscowo wyłącznie w okolice chorych tkanek i ubytków kostnych. Dzięki temu można by odejść od ogólnoustrojowego podawania leków na osteoporozę oraz aplikowania znacznie większych stężeń leku w bezpośrednie sąsiedztwo chorych tkanek i tym samym zwiększenia efektywności terapii.
- Komponenty naszego hydrożelu naśladują naturalny skład tkanki kostnej. Wśród jego składników jest między innymi kolagen, kwas hialuronowy oraz chitozan, czyli polisacharyd o udowodnionych właściwościach antybakteryjnych, przeciwzapalnych i przeciwbólowych. Oprócz tego w jego skład wchodzi kluczowy składnik nieorganiczny. Jest nim syntetyzowany przez nas układ cząstek krzemionki dekorowanych hydroksyapatytem, który w hydrożelu i projektowanej terapii pełni kilka istotnych i pożytecznych funkcji. Składowe hydrożelu, po jego wstrzyknięciu, już w organizmie, wiążą się ze sobą wiązaniami kowalencyjnymi. Właściwość ta pozwala podać hydrożel nieinwazyjną drogą, a cały materiał zachowuje swoją funkcjonalność, ponieważ nie ulega niekontrolowanej degradacji - wyjaśnia dr hab. Joanna Lewandowska-Łańcucka z Wydziału Chemii UJ, która pracowała przy projekcie.
- Wykorzystany w hydrożelu hydroksyapatyt w organizmach żywych stanowi główny, nieorganiczny budulec tkanki kostnej, wpływając na jej wytrzymałość. W naszym materiale pełni on analogiczną rolę. Minerał ten odpowiednio zagęszcza preparat, który po wstrzyknięciu łatwo przywiera do tkanki kostnej w miejscu ubytku i służy za podłoże dla osteoblastów, które odbudowują kość. To jednak tylko skromna część naszej innowacji. Prawdziwie przełomowe odkrycie dotyczy możliwości związania w hydrożelu alendronianu sodu, czyli popularnie stosowanego leku na osteoporozę, uzyskując w ten sposób wielofunkcyjny materiał o potencjale terapeutycznym. Dzięki tym właściwościom lekarze poprzez wstrzyknięcie hydrożelu będą mogli
aplikować lek bezpośrednio w chore miejsca, gdzie będzie on stopniowo uwalniany
- dodaje dr Adriana Gilarska, współtwórczyni wynalazku.
Preparat był już testowany na modelu mysim. Naukowcy dowiedli, że nie wywołuje on efektu toksycznego. Udowodniono też, że zachodzi naturalna angiogeneza, która daje możliwość realnego wykorzystania tego materiału jako bazy dla odbudowujących się tkanek kostnych. Potwierdziło się także, że podany w hydrożelu lek - alendronian sodu - jest uwalniany do organizmu stopniowo, co dodatkowo może zwiększać skuteczność leczenia.
- Pierwsze testy hydrożelu na liniach komórkowych i modelach zwierzęcych
wypadły bardzo obiecująco
. Na razie planujemy przeznaczyć ten materiał do projektowania terapii mniejszych ubytków kostnych, spowodowanych przede wszystkim osteoporozą, ale również różnego rodzaju urazami czy ubytków, jakie powstają na przykład w wyniku operacji neurologicznych. Materiał powinien więc zainteresować szerokie grono lekarzy reumatologów, ortopedów, jak również neurologów i stomatologów - mówi dr Gabriela Konopka-Cupiał, Dyrektor CITTRU - Centrum Transferu Technologii UJ.
Naukowcy poszukują obecnie
inwestorów
, którzy zaangażowaliby się w dalszy rozwój wynalazku. Równolegle pracują też nad dalszymi modyfikacjami krzemionki wykorzystywanej w jego składzie, tak by zwiększyć możliwości zarządzania przyszłymi planami leczenia osteoporozy.
- Dzięki uzyskanemu projektowi Tango V - ścieżka A, finansowanemu ze środków Narodowego Centrum Badań i Rozwoju, możemy w dalszym ciągu rozwijać naszą technologię. Udało nam się zsyntetyzować dekorowane hydroksyapatytem i odpowiednio sfunkcjonlizowane mezoporowate cząstki krzemionki, co pozwala zaadsorbować i związać w hydrożelu kilkukrotnie większą ilość leku na osteoporozę. Badania wykazały, że użycie tego rodzaju cząstek pozwoli nie tylko znacznie zwiększać stężenie alendronianu sodu w pobliżu chorych miejsc, ale że porowata struktura będzie spowalniać proces uwalniania leku, co może wydłużyć w czasie jego działanie. To oznacza, że w przyszłości lekarze będą mogli precyzyjnie projektować zarówno moc, jak i czasochłonność terapii, w zasadzie całkowicie eliminując skutki uboczne, jakie niesie z sobą ogólnoustrojowe podawanie leku. Ze względu na wydajniejszy załadunek lekiem, ale także, co warte podkreślenia, przyspieszony proces dekoracji hydroksyapatytem ta udoskonalona wersja bioaktywnego nośnika posiada znacznie większy potencjał aplikacyjny - wyjaśnia dr hab. Joanna Lewandowska-Łańcucka.

Zobacz też:
Hej, przypominamy tylko:
1. Szanujemy nawet ostrą dyskusję i wolność słowa, ale nie agresję. Przemocowe treści będą usuwane.
2. W komentarzach można swobodnie używać embedów z mediów społecznościowych.
3. Polecamy założenie konta, dzięki temu możesz zobaczyć wszystkie swoje dyskusje w jednym miejscu i dodać coś (👉 Sortownia), co trafi na stronę główną.
4. Jeżeli chcesz Donalda bez reklam, dołącz do naszych patronów: https://patronite.pl/donaldpl
NAJLEPSZE KOMENTARZE TYGODNIA
![Czechy: premier Babisz zapowiada odwrót od proukraińskiej polityki]()
![Wielka Brytania dopuściła pary jednopłciowe do startów w tańcach na lodzie]()
![Elon Musk niepokoi się o polską dzietność i zapowiada zapaść demograficzną]()
![Unia się odwinęła i wprowadza cło na chińskie paczki z Temu i Shein]() Więcej popularnych
Więcej popularnych
Popularne dzisiaj
Czechy: premier Babisz zapowiada odwrót od proukraińskiej polityki

40
"Nie będziemy udzielać żadnych gwarancji finansowych i nie będziemy nic dawać". Zobacz więcej »
Wielka Brytania dopuściła pary jednopłciowe do startów w tańcach na lodzie

26
Mowa o zawodach na szczeblu krajowym oraz niższym niż krajowy. Zobacz więcej »
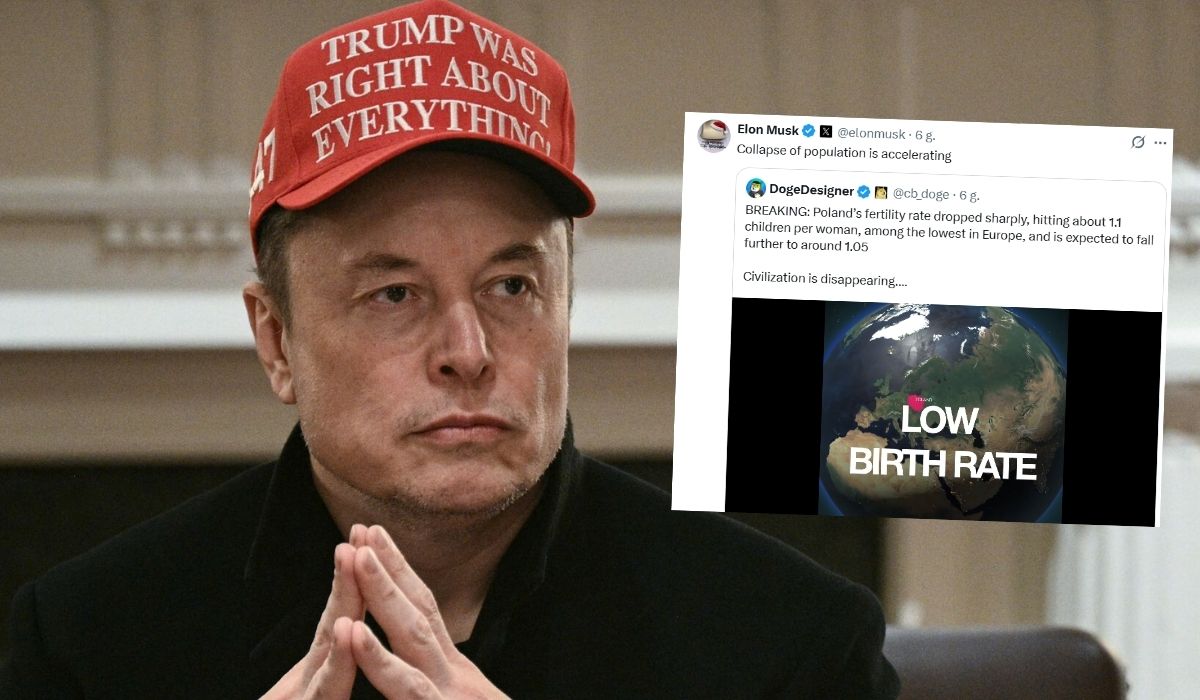
Elon Musk niepokoi się o polską dzietność i zapowiada zapaść demograficzną
62
"Przyspiesza się załamanie populacji". Zobacz więcej »
Unia się odwinęła i wprowadza cło na chińskie paczki z Temu i Shein

23
Opłata wyniesie 3 euro i będzie nakładana na produkty trafiające do UE w małych paczkach o wartości do 150 euro. Zobacz więcej »